Periodensystem
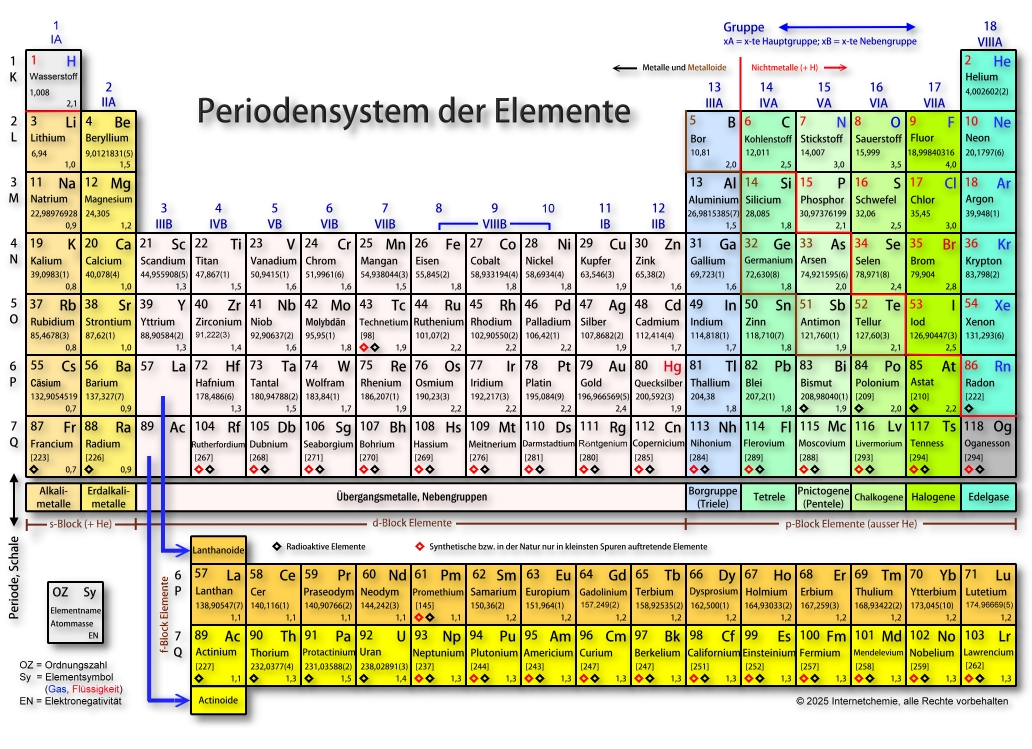
Ordnungszahl :
-
Die Elemente sind nach steigender Ordnungszahl von links nach rechts und von oben nach unten angeordnet.
-
Die Ordnungszahl ist gleich der Anzahl der Protonen im Atomkern.
-
Massen Zahl : Atomare Masse in u , entspricht der Nukleonen Zahl (Summe aus Protonen & Neutronen)

Perioden (Zeilen)
-
Die Periodennummer (1 bis 7) gibt die Anzahl der Elektronenschalen an, die das Atom im Bohr’schen Schalenmodell besitzt.
-
Innerhalb einer Periode nimmt die Zahl der Außenelektronen (Valenzelektronen) von links nach rechts zu (mit einigen Ausnahmen).
Gruppen (Spalten)
-
Gleiche Gruppe : Ähnliche Eigenschaften
-
Es gibt 18 Gruppen, unterteilt in Untergruppen
-
Hauptgruppen (1, 2 und 13–18) und Nebengruppen (3–12).
Einteilung:
- Das PSE kann in Metalle (links und Mitte), Nichtmetalle (rechts) und Halbmetalle (auf der Trennlinie) eingeteilt werden + (Edelgase)
Art der Bindung
Ionenbindungen (Salze)
-
KochSalz
NaCl -
Zur ERfüllung der Oktett Regel gibt einer ELektronen ab, der andere nimmt diese auf
- Der Aufnehmende meistens das Nicht-metall, Abgebende meistens ein Metall
Metall Bindungen
-
Beispiel : Silber :
Ag
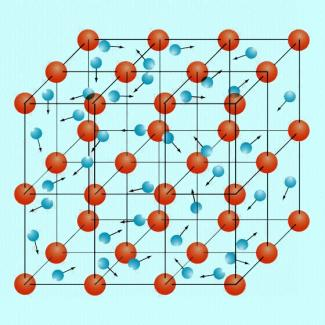
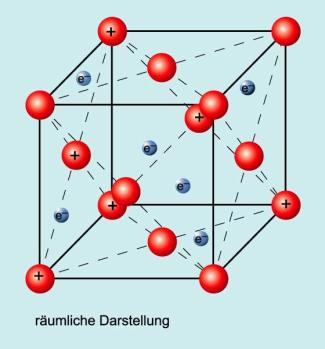
→ Beispiel Würfel
AtomRümpfe (Kugelpackung) + ElektronenWolken angeordnet -
Es gibt einen Valenzband & ein Leitungsband → diese Überlappen
-
Das Valenzband ist normalerweise vollständig gefüllt
-
Das Leitungsband ist vollständig leer
- Falls überlappend : sind Leiter
💡
Bei HalbMetallen : Leitungs- und Valenzband überlappen nicht.
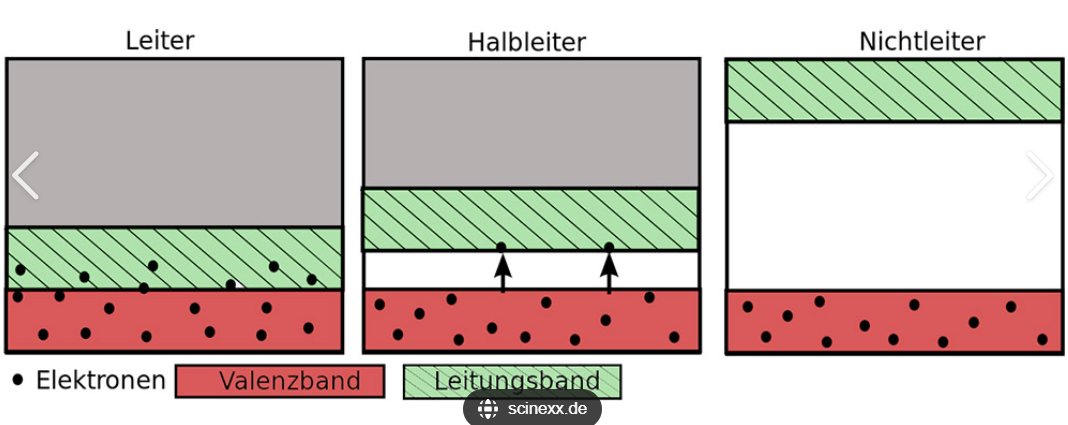
- Nicht Leiter sind oft Oxide → Ionenbindungen
Atom Bindung
-
Sind meistens Elemente mit ähnlicher Elektronegatovität
-
Sind ausschließlich Nicht-metalle
-
Nutzen Elektronen gemeinsam um die
Oktett-regelzu erfüllen -
Wird auch
chemische Bindung || Atombindunggenannt -
In diesem Fall benötiogt man die Hybridisierung der Orbitale
-
Organische Chemie
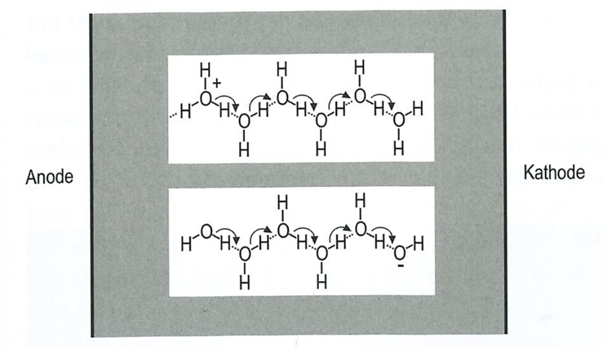
Beispiel : Wasser - H2O
Die Lewis Formel :
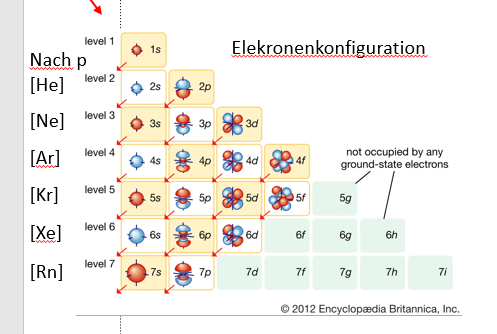
| Eigenschaft | Innerhalb einer Periode (links nach rechts) | Innerhalb einer Hauptgruppe (oben nach unten) |
| Elektronegativität | Nimmt zu (Atome ziehen Bindungselektronen stärker an) | Nimmt ab (Valenzelektronen sind weiter vom Kern entfernt) |
| Atomradius | Nimmt ab (stärkere Kernladung zieht Elektronen stärker an) | Nimmt zu (zusätzliche Elektronenschalen) |
| Ionisierungsenergie | Nimmt zu (mehr Energie nötig, um Elektronen zu entfernen) | Nimmt ab (Elektronen leichter entfernbar) |
| Metallcharakter | Nimmt ab | Nimmt zu |