Elektrochemie
💡
Elektrochemie befasst sich mit den chemischen
Reaktionen, die Elektrizität erzeugen oder durch Elektrizität angetrieben werden.
Beispiele können Batterien oder Akkus seinElektrolyse
Redox Reaktionen - 2 Reaktionen
Redox setzt sich aus zwei Teilen Zusammen :
-
einer Reduktion
(Elektronen e- werden aufgenommen) -
einer Oxidation
(Elektronen e- werden abgegeben)
Elektronenübergabe immer gekoppelt : Ein Partner oxodiert, der andere reduziert.
💡
Wichtig : Diese Zwei Reaktionen passieren immer
gleichzeitig
Ein Stoff gibt Elektronen ab, der andere nimmt diese auf.
Beispiel : Kochsalz - Natriumchlorid, NaCl
Natriumchlorid besteht aus : aus dem Metall Natrium Na und giftigem Chlorgas Cl_2.
Die Redox Gleichung
💡
Wir können nun die Gelchungen aufstellen :
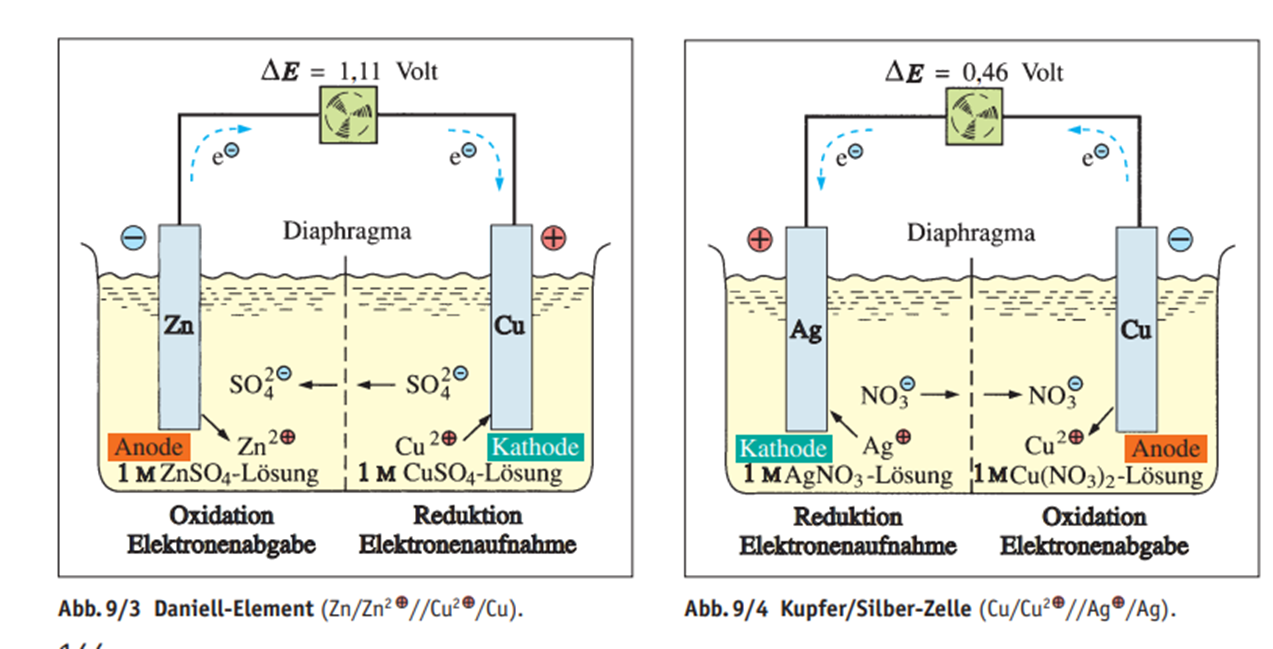
Elektrochemische Zellen
- Bestehen aus zwei Halbzellen, in denen Oxidation und Reduktion getrennt stattfinden.
-
Zwischen den Halbzellen fließen Elektronen durch einen elektsichen Leiter
-
Ionen wandern in Elektrolyten um den Ladungsausgleich herzustellen
-
💡
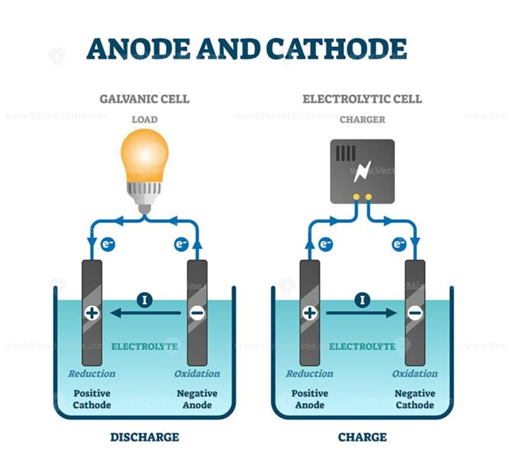
Beispiele :
Galvanische Zellen - Batterie
Elektrolysezelle - Nutzt Elektrische Energie um Reaktion zu erzwingen
Anwendungen
-
Batterien und Akkumulatoren
-
Korrosionsschutz
-
Elektrolyse (Herstellung von Metallen, Chlor, WasserStoff)
-
Biochemische Elektrochemie, z.B Zellatmung und photosynthetische Elektronentransportketten
Elektroden :
Anode
Hier findet die Oxidation statt, (Elektronen Abgabe)
Kathode
Hier findet die Reduktion statt (Elektronen Aufnahme)
In galvanischen Zellen fließen Leektronen von der Anode zur Kathode.
Hierbei wird die Rekation zur Stromgewinnung genutzt.
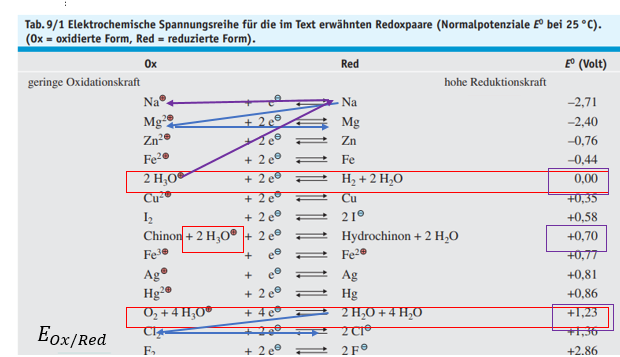
Nernst-Gleichung
-
Beschreibt die Abhängigkeit des Zellpotentials von den Ionenkonzentrationen.
-
Erlaubt Vorhersage, ob Reaktionen spontan ablaufen.